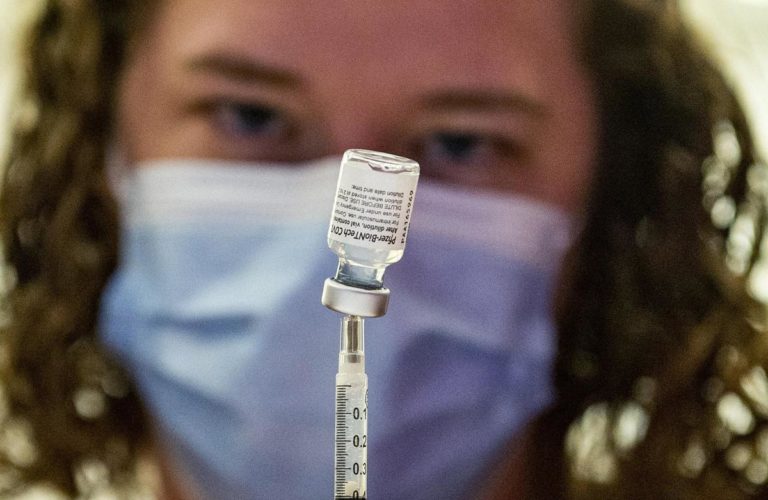
Via libera in Ue ai primi vaccini anti-Covid aggiornati a Omicron 1 proposti da Pfizer-BioNTech e Moderna. Il comitato per i medicinali a uso umano (Chmp) dell’Agenzia europea del farmaco Ema ha infatti raccomandato oggi di autorizzare due vaccini adattati per fornire una protezione più ampia contro Covid. Si tratta del vaccino Comirnaty*, bivalente e mirato a coprire il ceppo originario del virus e Omicron 1, e del vaccino Spikevax*, bivalente e anch’esso mirato a ceppo originario e Omicron BA.1.
I vaccini, spiega l’Ema nella nota in cui annuncia il verdetto, sono destinati all’uso in persone di età pari o superiore a 12 anni che hanno ricevuto almeno il ciclo di vaccinazione primaria contro Covid. Saranno quindi usati come booster. Questi vaccini sono versioni adattate dei vaccini originali Comirnaty* (Pfizer/BioNTech) e Spikevax* (Moderna).
L’Ema precisa che “i vaccini anti-Covid originali, Comirnaty e Spikevax, sono ancora efficaci nel prevenire malattie gravi, ospedalizzazioni e decessi associati a Covid e continueranno a essere utilizzati nelle campagne di vaccinazione nell’Ue, in particolare per le vaccinazioni primarie”.
Saranno “le autorità nazionali nei vari Stati membri dell’Ue a determinare chi dovrebbe ricevere il vaccino, quale vaccino fare e quando”. Mentre è già in corso la valutazione di uno dei prodotti scudo bivalenti adattati per le sottovarianti Omicron 4-5.
Ogni Paese dell’Unione deciderà dunque come usare i vari vaccini di volta in volta disponibili, modulando le proprie strategie vaccinali “tenendo conto di fattori quali i tassi di infezione e ospedalizzazione, il rischio per le popolazioni vulnerabili, la copertura vaccinale e la disponibilità di vaccini”, aggiunge l’Ema.
“Con l’evolversi della pandemia, la strategia dell’Ue è quella di disporre di un’ampia gamma di vaccini adattati destinati a diverse varianti di Sars-CoV-2, in modo che gli Stati membri abbiano una pluralità di opzioni per soddisfare le loro esigenze quando progettano le loro strategie di vaccinazione”,spiega l’Agenzia europea del farmaco. “Questo è un elemento chiave nella strategia generale per combattere la pandemia – argomenta l’ente regolatorio – in quanto non è possibile prevedere come si evolverà il virus in futuro e quali varianti circoleranno questo inverno”.
Proprio in quest’ottica, rimarca, “altri vaccini adattati che incorporano varianti diverse, come le sottovarianti Omicron BA.4 e BA.5, sono attualmente in fase di revisione da parte dell’Ema o saranno presentati a breve. E, se autorizzati, estenderanno ulteriormente l’arsenale di vaccini disponibili. I dati clinici generati per i vaccini bivalenti mirati al ceppo originario e a BA.1 raccomandati oggi “supporteranno la valutazione e l’autorizzazione di vaccini ulteriormente adattati”.
Tutti i diritti riservati. La riproduzione, anche parziale, è possibile soltanto dietro autorizzazione dell’editore.
L’utente, previa registrazione, avrà la possibilità di commentare i contenuti proposti sul sito dell’Editore, ma dovrà farlo usando un linguaggio rispettoso della persona e del diritto alla diversa opinione, evitando espressioni offensive e ingiuriose, affinché la comunicazione sia, in quanto a contenuto e forma, civile.